Связь константы диссоциации и степени диссоциации
Диссоциация в химическом контексте — это распад вещества на другие молекулы. Это слово происходит от латинского слова « dissociatio» , что означает «разделение». В научной номенклатуре диссоциация принимает различные определения, поскольку она встречается и в такой области, как психология. Мы, однако, сосредоточимся на значении диссоциации в химии. В зависимости от процесса и используемого в нем вещества мы можем выделить различные типы диссоциации. Наиболее распространенной является электролитическая диссоциация, однако термическая диссоциация также является не менее важным процессом.

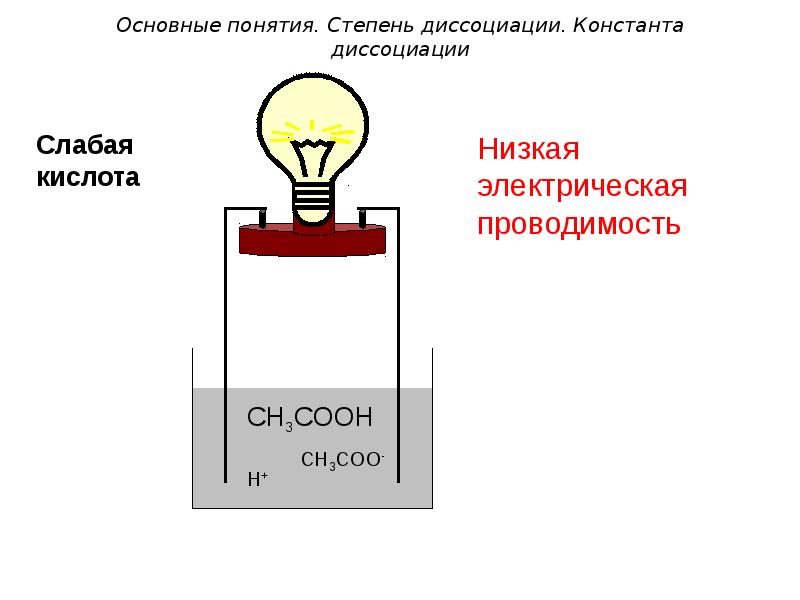





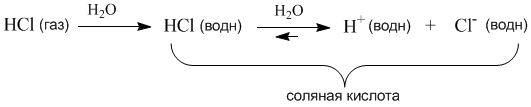
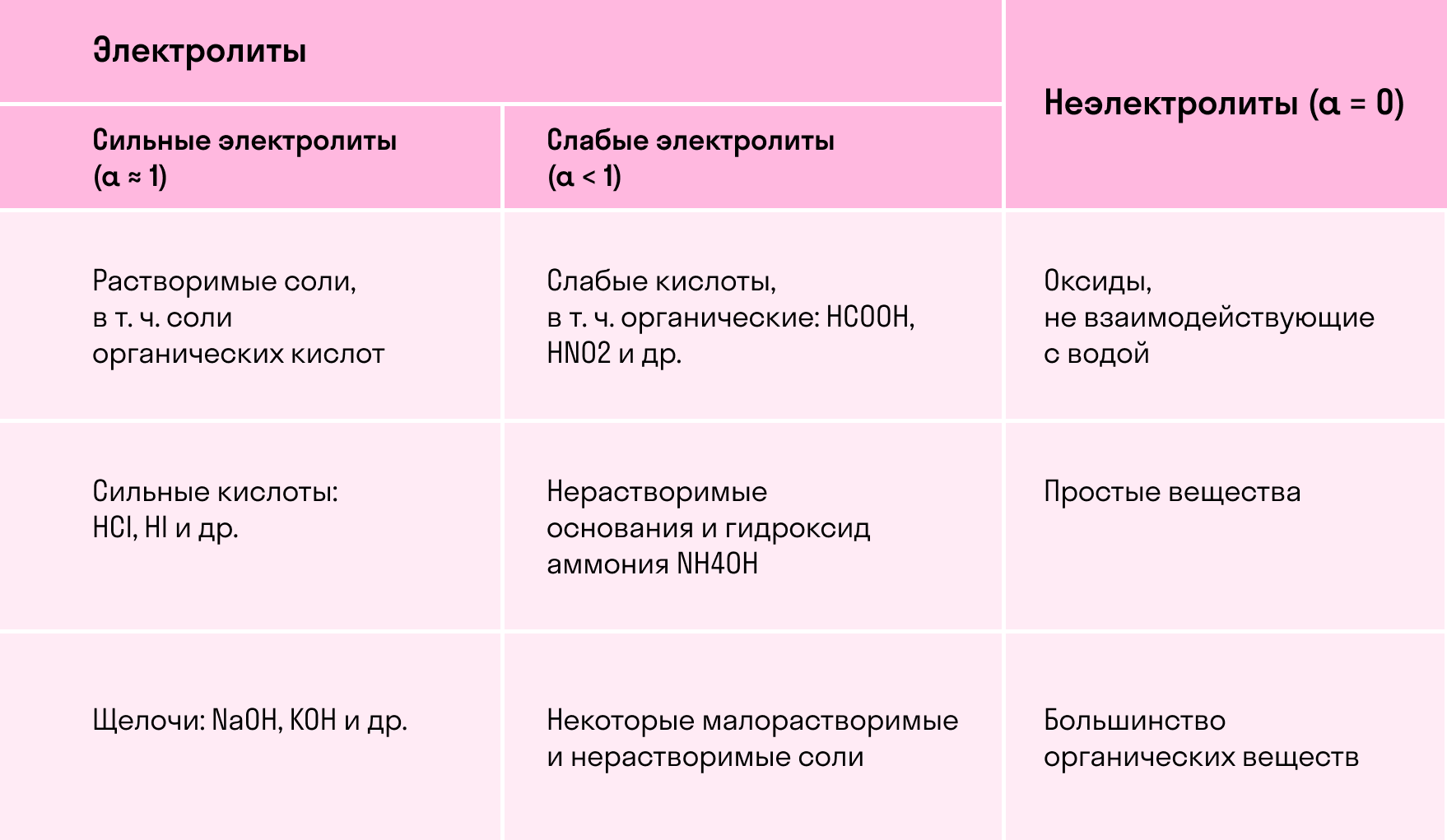
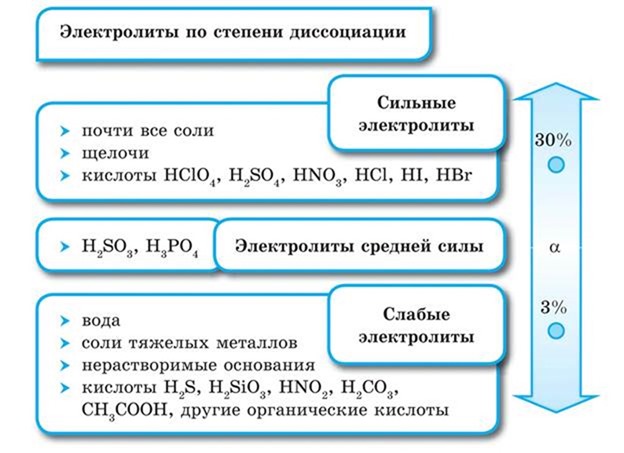
Известно, что существуют две основные причины прохождения электрического тока через проводники: либо за счёт движения электронов в электрическом поле, либо за счет движения ионов. Электрическая проводимость присуща, прежде всего, металлам. Ионная проводимость присуща многим химическим соединения, обладающим ионным строением, например, солям в твёрдом или расплавленном состояниях, а также многим водным и неводным растворам.

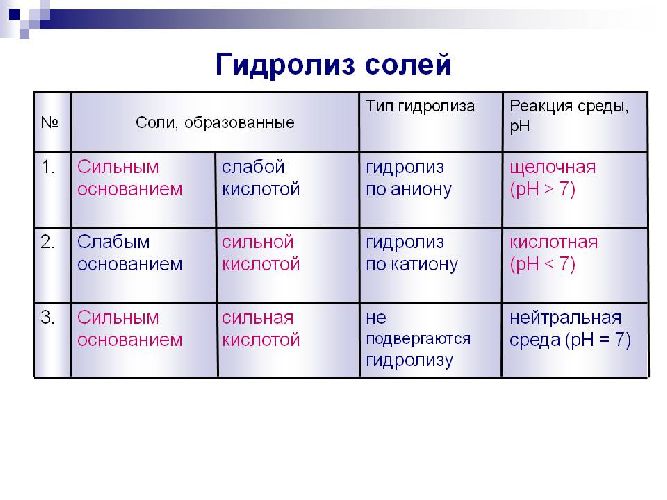


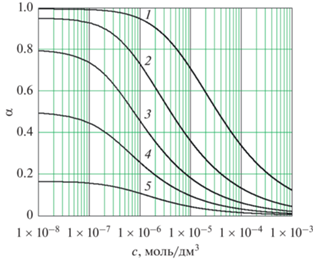



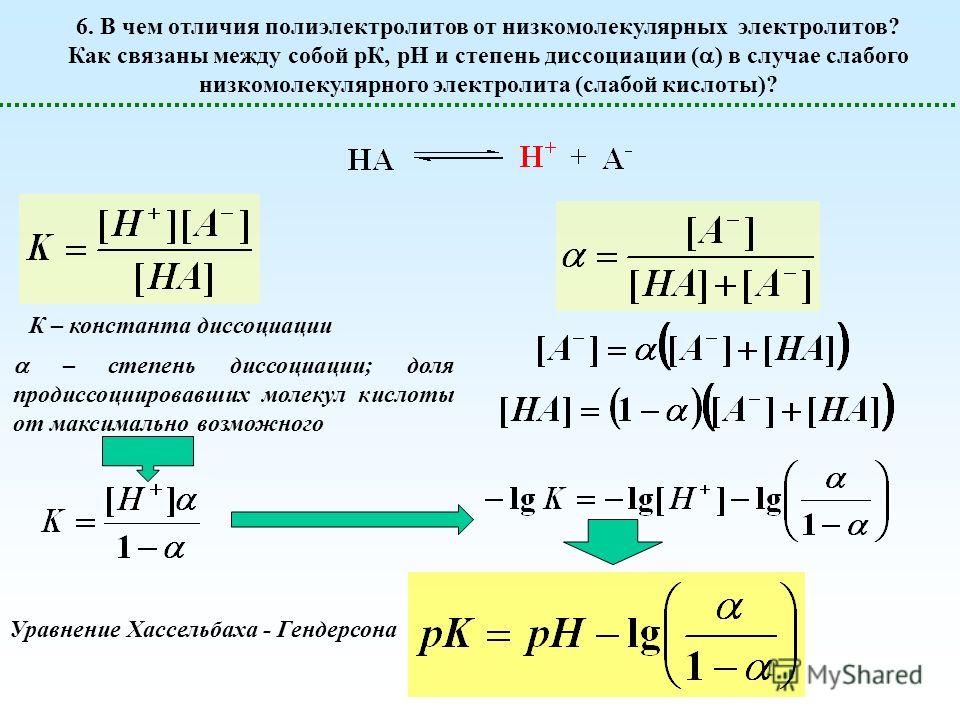
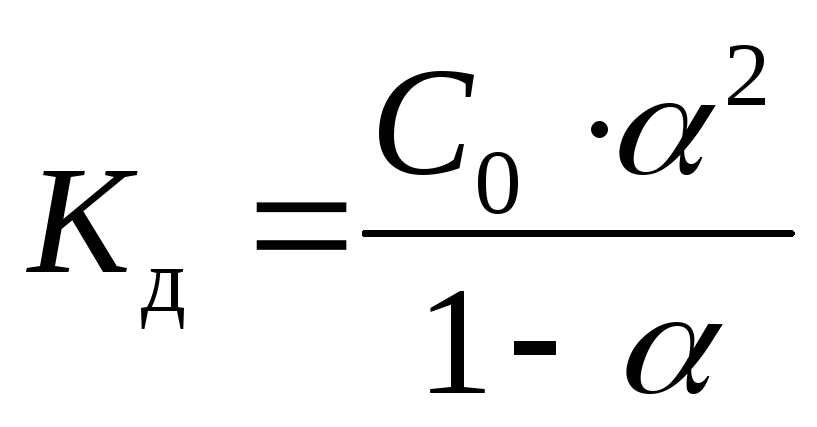

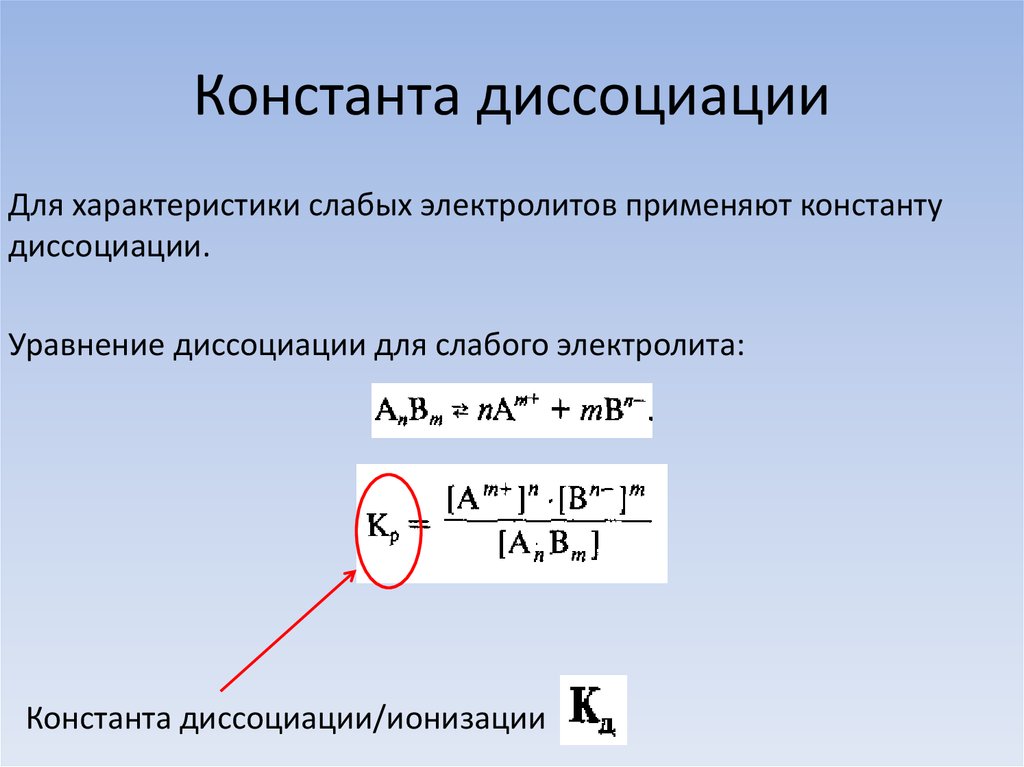
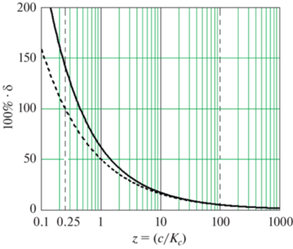
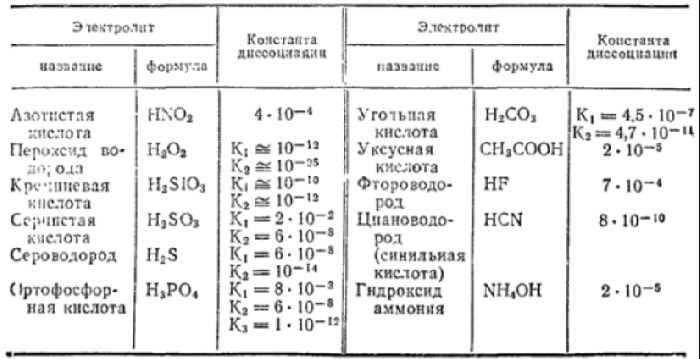
Закон действующих масс может быть применен к водным растворам кислот. Например, в водном растворе уксусной кислоты устанавливается следующее равновесие:. Величина Ка называется константой диссоциации кислоты. Константу диссоциации кислоты можно также выразить с помощью закона разбавления Оствальда:. Эту степень диссоциации можно установить, определяя молярные электропроводности раствора с заданной концентрацией, а также бесконечно разбавленного раствора подробнее об этом см. Константа диссоциации кислоты является мерой силы этой кислоты.